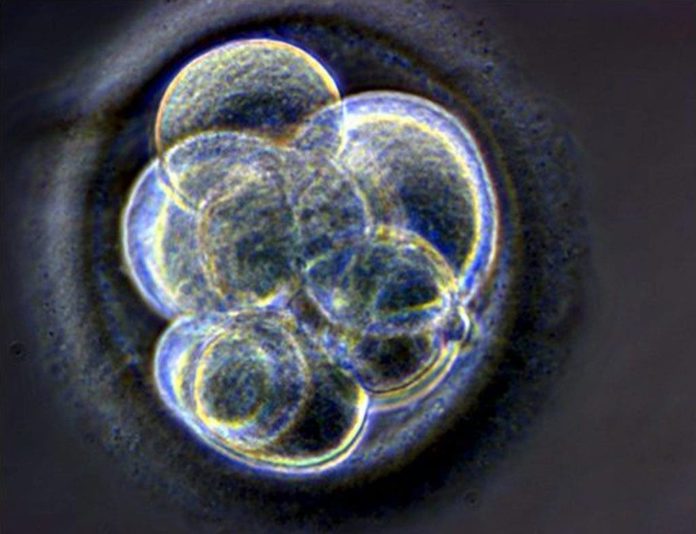
Les blastocystes, complexes et fascinants, sont de nouveau d’actualité : deux équipes de scientifiques ont créé en laboratoire des « structures semblables à des embryons » d’embryons précoces (blastocystes) à partir de cellules humaines.
Leurs défauts, ceux des blastocystes, sont l’une des causes des fausses couches et sont étroitement liés à l’échec de la reproduction.
D’où l’importance de toutes les recherches en cours dans le monde, comme les dernières citées ci-dessus, menées à l’Université Monash en Australie et à l’Université du Texas Southwestern (USA).
L’intérêt des blastocystes réside, entre autres, dans leur structure complexe composée d’environ 200 cellules qui se forment en quelques jours seulement après la fécondation de l’ovule.
Pour mieux comprendre le processus des blastocystes et de l’embryon, ainsi que les recherches des universités susmentionnées, le docteur Marcos Meseguer, superviseur scientifique et embryologiste à l’IVI (Institut valencien de l’infertilité) a répondu aux questions suivantes.
Blastocystes : premières heures d’un embryon.
Quelle est la structure cellulaire des blastocystes ?
Les blastocystes sont la première structure complexe à se former au cours du développement de l’embryon, environ 110 heures après la fécondation.
Il se compose de trois parties fondamentales :
1. une couche externe de cellules appelée trophoectoderme (qui formera le placenta).
2 – Un groupe interne de cellules appelé la masse cellulaire interne à partir de laquelle le fœtus se formera.
3. une cavité interne appelée blastocèle, le tout entouré d’une structure protectrice appelée zone pellucide.
Ses défauts sont-ils l’une des causes des fausses couches ?
Oui, elles le sont ; les causes des fausses couches sont multiples, à de nombreuses reprises nous les associons à des anomalies chromosomiques (un nombre excessif de chromosomes ; pertes ou gains totaux ou partiels).
Mais les raisons peuvent aussi être autres (défaillances au niveau cellulaire ou moléculaire), certaines connues et beaucoup d’autres encore inconnues.
Quel type d’études ou de connaissances la création en laboratoire des « iBlastocytes » à l’université Monash permettra-t-elle ?
En théorie, il s’agit des mêmes études que celles que l’on pourrait faire avec de vrais embryons, mais sans les inconvénients éthiques et juridiques que comporte une telle recherche.
Néanmoins, en Espagne, la recherche sur les embryons est possible, avec les embryons restants des traitements de reproduction assistée.
Il s’agit d’embryons que les patients donnent pour la recherche dans le cadre de projets préalablement approuvés par un comité d’éthique et par la Commission nationale d’assistance à la procréation.
Il se pourrait qu’un projet non approuvé par ces organismes avec des embryons réels soit autorisé avec ces « iBlastocytes », mais il s’agit d’une situation hypothétique.
Ces derniers possèdent-ils un énorme potentiel pour comprendre l’infertilité et la perte précoce de grossesse ?
Ils possèdent peut-être un potentiel similaire à celui des embryons réels pour acquérir ces connaissances, mais je n’en pense pas plus.
Pour les scientifiques, du moins en Espagne, la disponibilité des embryons pour la recherche n’est pas un facteur limitant, les ressources économiques et les limites éthiques que la loi fixe, mais pas la disponibilité.
Blastocytes : de nombreuses inconnues.
Y a-t-il encore beaucoup d’inconnues à ce sujet ?
Oui, il y en a encore beaucoup, nous ne savons pas pourquoi certains embryons sont arrêtés dans leur développement à des stades précoces.
Cependant, nos connaissances ont considérablement augmenté ces dernières années, notamment grâce aux nouvelles techniques non invasives. Nous sommes capables d’observer en détail chaque minute du développement de l’embryon, de savoir ce qu’il utilise et libère dans le milieu de culture où il se développe, et tout cela sans manipuler l’embryon, sans altérer son développement, sans l’endommager.
En outre, l’intelligence artificielle nous aide à beaucoup mieux comprendre le développement de l’embryon et à découvrir des schémas spécifiques associés à l’échec de la reproduction.
Quant aux blastoïdes, également obtenus en laboratoire à partir de cellules souches pluripotentes humaines (Université du Texas), quels types d’avancées ou d’études permettent-ils ou permettront-ils ?
Les études potentielles sont les mêmes que celles développées en Australie, c’est-à-dire qu’il s’agit de modèles expérimentaux in vitro qui permettent toutes sortes d’études fonctionnelles.
Ces études peuvent nous aider à connaître les causes des altérations du développement embryonnaire, c’est-à-dire un blocage ou un développement irrégulier ou atypique.
Quels aspects du développement humain précoce sont capables de récapituler des structures de type blastocyste ?
Le développement embryonnaire précoce est connu dans ses moindres détails, grâce aux nouvelles technologies appliquées ces dix dernières années, par exemple le time-lapse.
Le fait qu’ils soient connus en détail n’implique pas nécessairement que tous les aspects moléculaires et cellulaires qui régulent les principaux événements du développement embryonnaire que nous avons si minutieusement observés soient connus.
À cet égard, par exemple, des modèles animaux ont été utilisés pour connaître les gènes liés aux cycles cellulaires, aux schémas de division, à la différenciation des cellules embryonnaires, etc…..
L’expérimentation animale a été la principale source de connaissances sur la reproduction assistée et l’origine de la plupart des techniques de fécondation in vitro que nous, embryologistes, pratiquons dans notre routine clinique.
Ces nouvelles avancées peuvent sans doute constituer une nouvelle source de connaissances à ajouter.
Quelles limites et quels avantages voyez-vous dans cette technologie ?
Eh bien, en soi, les modèles de culture d’embryons « IN VITRO » ne doivent pas être exactement les mêmes, dans le temps et dans la forme, que le développement « in vivo », mais ils constituent une approximation très proche qui nous a permis de progresser considérablement dans les techniques de reproduction assistée et dans la résolution des problèmes d’infertilité.
Les modèles proposés ici sont probablement encore plus éloignés du développement in vivo et, par conséquent, leur extrapolation à la réalité cellulaire pourrait être encore plus éloignée.
Néanmoins, il s’agit d’une grande avancée technologique, le développement de ce modèle a un énorme mérite scientifique qui ne fait que valoriser l’énorme niveau de ces chercheurs qui les a placés à l’avant-garde mondiale de la biologie cellulaire, et nous ressentons une grande admiration pour tout leur travail.